Glycosidases
Glycosidases
Overview
糖基化(Glycosylation)是存在於真核生物蛋白質中最常見的翻譯後修飾(PTM)。
蛋白質上的糖基化結構具有多樣化功能,並可作為疾病生物標誌,例如用於監測癌症進程。因此,能夠促進醣蛋白特性解析(Glycoprotein characterization)的工具至關重要。
內切醣苷酶(Endoglycosidases)與外切醣苷酶(Exoglycosidases)是用於醣蛋白結構與功能分析的重要工具。其中,內切醣苷酶如PNGase F與Endo H,常用於去除N-醣基化蛋白(N-glycosylated proteins)上的醣鏈。
對於O-glycosylated proteins的分析,則建議使用內切與外切醣苷酶的混合處理方式。
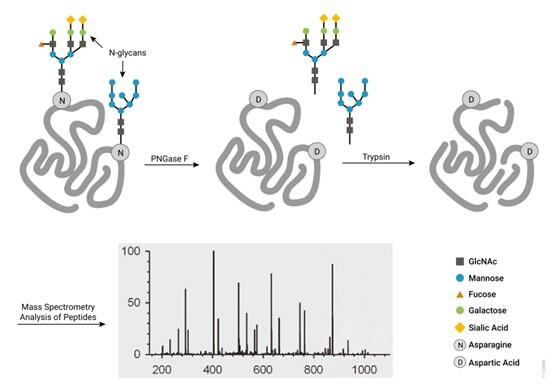
▲蛋白質中N-醣基化位點的鑑定Asn連接的醣鏈可透過PNGase F進行酵素切除,產生完整的寡醣結構以及去醣基化的蛋白質。在此過程中,位於N-醣基化位點的Asn residues會轉換為Asp。
Glycosidases
- 透過LC-MS/MS鑑定醣基化位點
- 醣蛋白與醣鏈結構之特性分析
- 蛋白質運輸路徑監測(內質網、高基氏體)
- 結構與功能相關性研究
Endo H
Endo H為一種Recombinant glycosidase,來源於Streptomyces plicatus並於E. coli中過量表現。Endo H可切割N-linked glycoproteins中High mannose及部分混合型Hybrid寡醣的Chitobiose核心結構內部鍵結。
與PNGase F不同,Endo H 無法切割複雜型Complex type N-醣基化蛋白。Endo H 的酵素作用會在蛋白質的N-醣基化位點留下一個GlcNAc殘基,導致分子量(M.W.)改變。此分子量變化可用於質譜分析中,作為N-醣基化位點鑑定的依據。
PNGase F
PNGase F為一種Recombinant glycosidase,來源於Elizabethkingia miricola,並於E. coli中過量表現,其分子量約為36 kDa。
PNGase F可催化N-linked oligosaccharides的切割,作用於最內層 N-Acetylglucosamine (GlcNAc)與Asparagine residues (Asn)殘基之間的鍵結,適用於High mannose型、Hybrid及Complex oligosaccharides。
在酵素作用後,完整寡醣會被釋放,而原本的Asn殘基會轉換為Asp。此去胺反應Deamination造成+0.9840 Da的單同位素質量變化,可用於串聯質譜(MS/MS)中N-linked glycoproteins的鑑定。
PNGase F無法移除含α-(1,3) 鍵結核心Core fucose的寡醣結構,此類結構常見於植物來源的醣蛋白。
Fetuin
Fetuin為一種同時具有O-連結與N-連結醣基化位點的醣蛋白,可作為PNGase F與Endo H去醣基化酵素活性監測的Substrate control。
▲PNGase F與Endo H對N-glycans的切割專一性
▲SDS-PAGE中N-glycosylated蛋白的偵測
在移除醣鏈後,相對應的蛋白質於SDS-PAGE中會呈現較高的遷移率(Mobility 提升)。如圖所示,對於Immunoglobulin G (IgG),同時應用 PNGase F (A圖)與 Endo H (B圖),可用於判定是否存在複雜型醣鏈結構(Complex glycan structures),具有重要分析資訊價值。